- 文章

- 研究观点
- 颠覆性技术
中国生物科技行业 中国创新药物的DeepSeek时刻?
汇丰前海证券中国医疗行业分析师柴欣然认为PD(L)1 双抗具有成为抗肿瘤标准治疗的潜力,中国创新药物或迎来DeepSeek时刻。
中国生物科技是今年市场热度最高、持续上扬的板块。恒生生物科技指数(其成分股包括50家最大的香港上市生物科技公司)年初至今上涨91%,远超基准恒生指数同期26%的涨幅。我们认为这得益于中国生物科技公司在创新药研发取得的巨大进步。
中国生物科技企业开发了一种新型癌症免疫治疗法双抗靶向PD(L)1。PD(L)1双抗被视为下一代 PD(L)1,因为这些药物可以同时结合两个不同的靶点,从而增强免疫反应。这可能会增强抗肿瘤活性,克服PD(L)1 抑制剂的耐药性,并扩大采用该方法治疗的癌症范围。中国的临床研究发现,由中国创新药公司开发的依沃西单抗(Ivonescimab)在一项治疗肺癌的中国三期临床实验中疗效战胜默沙东研发的全球最畅销创新药Keytruda(可瑞达)(资料来源:彭博,2025年7月13日),因此被喻为中国生物科技行业的DeepSeek时刻。
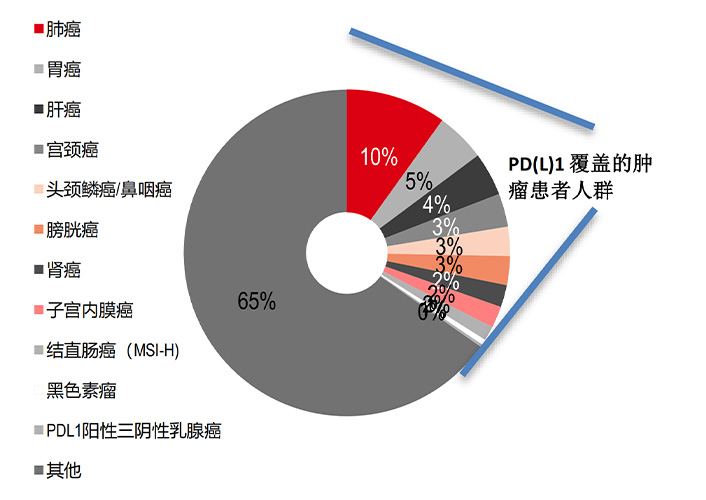
传统PD(L)1目前仅覆盖三分之一的实体瘤患者…
资料来源:弗若斯特沙利文、全球癌症数据库2022、公司资料、医药魔方、汇丰前海证券估测
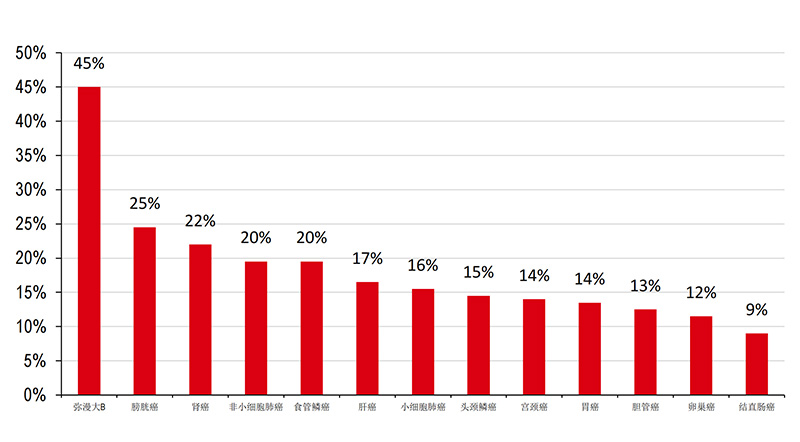
… 且抗肿瘤疗效一般
资料来源:公司资料、全球癌症数据库2022、医药魔方、汇丰前海证券
中国生物科技公司在PD(L)1双抗市场占据主导地位。该市场的前五大资产分别是AK112(康方生物/Summit)、BNT327(BioNTech/百时美施贵宝)、SSGJ707(三生制药/辉瑞)、LM299(默沙东)和IBI363(信达生物),所有这些资产都得到强大的数据积累的支持,且均有正在进行中或计划中的注册性III期临床试验。AK112取得成功后,生物科技和生物制药公司目前正优先研发PD(L)1双抗资产,多项前线治疗实体瘤的临床试验正在进行中。目前有300多款PD(L) 1双抗候选药物正在研发中,约90款已进入临床阶段,主要来自中国药企(资料来源:公司资料、医药魔方)。
中国企业具有先发优势,有助于其与跨国药企达成更多重大交易。在全球市场,仅AK112和BNT327分别已于2023 年下半年和2025年上半年启动全球注册性III期临床试验。在中国市场,AK112和AK104已经上市,探索更广泛适应症的多项 III 期临床试验正在进行中。SSGJ707、IBI363和BNT327于2024年下半年至2025年启动注册性III期临床试验(资料来源:公司资料、医药魔方)。
尽管大多数PD(L) 1双抗候选药物由中国企业开发,但鉴于发达市场更有利的定价、有限的竞争及其高度发达的商业保险体系,我们认为这些候选药物海外上市或能最大限度地挖掘其商业价值。全球制药巨头面临着迫在眉睫的“专利悬崖”,因此对研发下一代疗法兴趣浓厚。双抗正在引起全球投资者的兴趣。此前与中国生物科技公司达成授权合作,或计划未来参与合作的跨国药企对中国创新药高度关注。最近的一些发展动态和交易活动将PD(L)1双抗推向焦点:(1)由康方生物和美国Summit Therapeutics公司共同开发的用于治疗肺癌的Akeso AK112国内与海外三期临床疗效数据令人鼓舞。(2)三生制药与辉瑞就SSGJ707 (PD1/VEGF)达成授权协议,交易额超60亿美元。(3)百时美施贵宝和BioNTech就BNT327 (PDL1/VEGF)达成合作开发协议,交易额达创纪录的111亿美元。
以下主要负责撰写本文的分析师声明,本文中表达的观点及预测均准确地反映了他们的个人观点,他们过去、现在或将来的薪酬均与本文中的具体建议或观点没有直接或间接关系:柴欣然(登记编码:S1700523040001)、舒影岚(登记编码:S1700522120001)。
本文由汇丰前海证券有限责任公司(“汇丰前海”)的研究部发布。
汇丰集团及其关联机构将不时以当事人或代理人的身份,向客户卖出或从客户手中买入汇丰集团研究覆盖的证券,如股票和债券(包括衍生品)。
分析师、宏观经济分析师和策略分析师所得报酬,部分参照了包括投资银行、销售交易、自营交易收入在内的汇丰集团盈利能力情况。
我们不会事先决定是否或在某个时间段内发布一份更新报告。
本文提及的有关任何公司的披露信息,请登录 https://www.hsbcnet.com/research 参阅该公司的最新报告。
其他披露信息
- 本文节选自汇丰前海已于2025年8月29日发布的研究报告,具体分析内容(包括相关风险提示)请详见相关研究报告。
- 本文中的所有市场数据截至2025年8月27日,除非在本文中已注明了其他特定日期及/或某天的特定时间点。
- 汇丰集团设有识别及管理与研究业务相关的潜在利益冲突的制度。汇丰集团分析师及其他从事研究报告准备和发布工作的人员有独立于投资银行业务的管理汇报路线。研究业务与投资银行及自营业务之间有信息隔离墙,以确保保密信息和(或)价格敏感性信息可以得到妥善处理。
- 您不可出于以下目的使用/引用本文中的任何数据作为参考:(i)决定贷款协议、其他融资合同或金融工具项下的应付利息,或其他应付款项,(ii) 决定购买、出售、交易或赎回金融工具的价格,或金融工具的价值,和/或 (iii) 测度金融工具或投资基金的表现。
本文由汇丰前海证券有限责任公司(“汇丰前海”)发布。本文基于汇丰前海认为来源可靠的资料编制,但所用资料未经独立核实。汇丰前海受中国证券监督管理委员会(“中国证监会”)监管,具有中国证监会核准的证券投资咨询业务资格,业务许可证编号:【91440300MA5EPLHG1B】。所有与本文相关的查询须联系您在汇丰前海的联系人。汇丰前海或任何其集团公司成员(“汇丰”)对有关资料的准确性或完整性概不作任何担保、陈述或保证,也不会对此承担任何责任或义务,亦不就传递的事实或分析资料的错误负责,亦不会就任何人因依赖该等资料而引致的损害负责。本文所载资料及意见乃以刊发时的公开资料为准,乃汇丰现时之判断,如有更改,恕不另行通知。
本网站不是汇丰前海研究报告的发布平台。本文涉及的研究报告信息是基于汇丰前海已发布的研究报告编制而成。投资者只有在了解了相关研究报告中的全部信息基础上,才可能对研究报告所表达的观点形成比较全面的认识。本文仅为对相关研究报告部分内容的引用或者复述,因受技术或其他客观条件所限无法同时提供观点形成的依据等相关信息,其内容无法完整或准确表达相关研究报告的观点或意见。
本文仅用作信息参考之目的,不应视作卖方要约,也不能被视为买方要约或诱使买入证券或文中提到的其他投资产品的要约,和(或)参与任何的交易策略。本文不构成招股说明书或其他发行材料。由于本文的撰写并不考虑任何特定投资者的目标、财务状况或需要,因此本文中的建议是一般性的,并不代表个性化建议。相应地,投资者在依建议进行操作之前,要根据自身的目标、财务状况和需要,考虑所给出建议的恰当性。如需要,可获取专业的投资和税收建议。
投资者须自主做出是否买入、认购或卖出(如适用)的投资决定并自行承担投资风险。在任何情况下,汇丰集团的任何成员均不会就因依赖本文的任何资料及材料而引致或与之相关的任何直接或间接或任何其他种类的损害向接收人承担任何责任。
特定投资产品过去的表现并不预示未来的表现。任何投资或收入的价值可能会下降或上升,您可能无法收回全部投资金额。如果投资以接收人的当地货币以外的货币计价,则汇率的变化可能会对该投资的价值、价格或收入产生不利影响。如果投资没有公认的市场,投资者可能难以出售其投资或获得有关其价值或风险程度的可靠信息。本文中包含的某些陈述可能被视为前瞻性陈述,提供对未来事件的当前预期或预测。此类前瞻性陈述并非对未来业绩或事件的保证,并涉及风险和不确定性。由于各种因素,实际结果可能与此类前瞻性陈述中描述的结果存在重大差异。
本文仅供参考,不得出于任何目的直接或间接地全部或部分重新分发或传递给任何其他人。本文在其他司法管辖区的分发可能受到法律的限制,拥有本文的人应了解并遵守任何此类限制。接受本文,即表示您同意受上述说明的约束。若本文发送至汇丰前海关联机构的任一客户,则向该接收人的提供须受接收人与该关联机构之间达成的商业条款约束。本文旨在全文分发。除非适用法律另有许可,否则如欲使用汇丰集团服务进行本文所述任何投资的交易,请联系所在司法管辖区的汇丰集团成员。
本文提到的某些投资产品可能不具备在某些国家和地区进行销售的资格,因此它们并不适用于所有类型的投资者。有关本文中提到的投资产品的适当性问题,投资者应咨询其汇丰集团代表。
本网站供中国大陆地区使用。本网站内提供的产品及信息供位于中国大陆地区的客户访问。如果您身在中国大陆地区以外的其他国家或地区,汇丰前海不能保证能根据您所身处或居住的国家或地区的相关法律法规而向您提供本网站下的相关产品和服务。本网站上提供的资料无意被任何人传递至或使用于相关法律法规限制或禁止传播或使用该等资料的任何国家或地区,也无意供该等国家或地区的人们使用。
任何涉及本文或其分发而引起的争议均适用中华人民共和国法律,并应受中华人民共和国境内具有管辖权的法院排他管辖。
©版权所有 2025 汇丰前海证券有限责任公司,不得转载。未经汇丰前海证券有限责任公司的事先书面许可,不得对本文任何部分进行复制、存储于检索系统,或以任何电子、机械、影印、记录或其他形式或方式进行传输。